重組生長因子是現代生命科學研究中不可或缺的重要工具,它們通過基因工程技術在體外表達和純化獲得,為細胞生物學、發育生物學及信號轉導研究提供了高純度、高活性的關鍵試劑。作為科研試劑,重組生長因子以其精確的序列一致性、可擴展的生產規模和卓越的批間一致性,顯著推動了基礎研究的標準化進程。本文將從技術層面系統介紹重組生長因子的基本特性、作用機制及典型應用場景。
生長因子是一類能夠調節細胞增殖、分化、遷移和存活的信號分子。在生理狀態下,它們以極低的濃度發揮作用,通過與細胞表面特異性受體結合,激活細胞內信號級聯反應,從而精確調控細胞行為。然而,天然來源的生長因子存在提取難度大、純度低、來源有限等問題,限制了其科研應用。重組DNA技術的出現徹底改變了這一局面。通過將編碼特定生長因子的基因克隆至表達載體(如大腸桿菌、哺乳動物細胞或酵母系統),研究人員能夠大規模生產結構明確、活性穩定的重組生長因子。
重組生長因子的核心特徵在於其分子結構的精確性。以重組人表皮生長因子(rhEGF)為例,其一級結構由53個氨基酸殘基組成,包含三對高度保守的二硫鍵,這些二硫鍵對其空間構象和生物活性至關重要。通過重組技術生產的rhEGF,其氨基酸序列與內源性EGF完全一致,且通過質譜分析和N端測序等技術嚴格驗證,確保了其結構與功能的真實性。類似地,其他常見重組生長因子,如成纖維細胞生長因子(FGF)、血管內皮生長因子(VEGF)、轉化生長因子-β(TGF-β)等,均具有特定的結構域和修飾(如糖基化),這些特徵直接影響其與受體的結合親和力和下游信號的特異性。
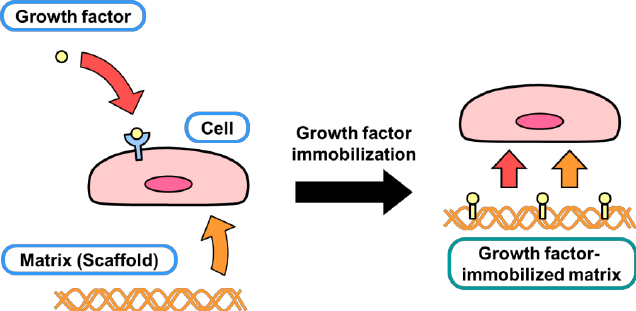
從作用機制角度看,重組生長因子主要通過自分泌、旁分泌或內分泌方式與靶細胞膜上的特異性受體相互作用。例如,重組人FGF基本型(rhFGF-basic)主要與成纖維細胞生長因子受體(FGFR)結合,誘導受體二聚化及自磷酸化,進而激活RAS/MAPK、PI3K/AKT及PLCγ等多條信號通路,最終調控細胞週期進程和基因表達。這種高度特異性的相互作用使得研究人員能夠在體外模型中精確操控細胞命運,例如在幹細胞培養中,通過添加特定組合的重組生長因子(如rhFGF-2、rhTGF-β1和rhBMP-4),可定向誘導其向特定譜系分化。
在科研應用中,重組生長因子已成為多種實驗體系的標配試劑。在細胞培養領域,它們被廣泛用作培養基添加劑,以支持原代細胞和細胞系的體外擴增。例如,在間充質幹細胞(MSC)培養中,重組人FGF-2被證實能夠有效延緩細胞衰老,維持其多向分化潛能。在三維細胞培養和類器官模型中,重組生長因子(如rhEGF、rhNoggin)的梯度分佈對於模擬體內微環境、引導細胞自組織形成複雜結構至關重要。此外,在信號轉導研究中,高純度的重組生長因子使得科學家能夠通過外源性添加或撤除,精確剖析特定通路在生理及病理過程中的作用,例如利用重組人VEGF-A165研究血管生成的分子機制。
為確保重組生長因子在科研中的可靠性,其質量控制環節尤為關鍵。儘管本文不涉及具體制備方法,但需要指出,通過ELISA、Western Blot、質譜及細胞增殖/分化報告基因檢測等多種技術,可對其純度、濃度、內毒素水平及生物活性進行全面評估。例如,通過NIH/3T3細胞增殖實驗可定量測定rhFGF-2的比活性,確保其在不同實驗批次間的一致性。
隨着多組學技術和精準醫學的發展,重組生長因子的應用場景正不斷拓展。在藥物篩選平台上,重組生長因子被用於構建更貼近生理狀態的疾病模型,如腫瘤微環境模擬系統。在蛋白質相互作用研究中,帶有標籤(如His、GST)的重組生長因子則為免疫共沉澱、表面等離子共振等技術提供了標準化探針。
總之,重組生長因子作為經過工程化改造的生物試劑,以其結構明確、活性可控、應用靈活的特點,已成為現代生命科學研究的基石工具。深入理解其分子特性與作用機制,將有助於科研人員更精準地設計實驗、解讀數據,並推動基礎研究向更深層次發展。
參考文獻
1.Aaronson, S. A. & Bottaro, D. P. A receptor tyrosine kinase mediated pathway in fibroblast growth factor signal transduction. Nature 343, 78-80 (2014).
2.Chen, L. et al. Recombinant human epidermal growth factor: production and applications in wound healing. Sci. Rep. 6, 21045 (2016).
3.Derynck, R. & Zhang, Y. E. Smad-dependent and Smad-independent pathways in TGF-β family signalling. Cell 118, 815-826 (2015).
4.Yancopoulos, G. D. et al. Vascular-specific growth factors and blood vessel formation. Nature 407, 242-248 (2012).
5.Zhang, J. & Li, L. Stem cell niche: structure and function. Annu. Rev. Cell Dev. Biol. 21, 605-631 (2015).